
《鬼道》致富:投資台灣生技,不可或缺的一環!
投資台灣生技:新藥(藥華藥)、非新藥(保瑞、美時、漢達、智擎)、再生醫療(長聖)、CDMO(保瑞)、原料藥(旭富)、醫材(晉弘)、通路(大樹、大學光)、保健(晨暉)……
其中,不可或缺的一環,就是剛通過立法院三讀的
《再生醫療法》及《再生醫療製劑管理條例》
簡單說
《再生醫療法》由衛福部醫事司主管,是管醫院和管技術的,取代了2018年的特管法:自體細胞療法(CAR-T,抽病人的免疫細胞出來培養之後打回去)。
規範醫療機構執行再生醫療技術(或)使用再生醫療製劑時,確保安全、品質及有效性,也限制臨床應用能執行再生醫療的範疇、再生醫療人體試驗及研究、組織細胞來源管理等等。
《再生醫療製劑管理條例》由衛福部食藥署(TFDA)主管,是管生技廠商和藥品的核准與否。
再生醫療雙法三讀版本的六大重點
重點一:限制異種細胞來源
恩慈療法排除異種細胞!
「鬼叔」:
恩慈療法可以用自體細胞療法(CAR-T, Autogenic)&異體細胞療法(抽「別人」的細胞來培養),如長聖的CAR001&UMSC01都是異體細胞療法(Allogenic),但是恩慈療法只能收成本費,對投資人不算利多!(異種細胞= 抽「其他動物」的細胞來培養,Xenogenic)
重點二:免人體試驗的規範和例外
除恩慈療法&原「特管法」核准的自體細胞療法(CAR-T)之外,必須完成人體試驗!

《鬼道》致富:投資台灣生技,不可或缺的一環!
投資台灣生技:新藥(藥華藥)、非新藥(保瑞、美時、漢達、智擎)、再生醫療(長聖)、CDMO(保瑞)、原料藥(旭富)、醫材(晉弘)、通路(大樹、大學光)、保健(晨暉)……
其中,不可或缺的一環,就是剛通過立法院三讀的
《再生醫療法》及《再生醫療製劑管理條例》
簡單說
《再生醫療法》由衛福部醫事司主管,是管醫院和管技術的,取代了2018年的特管法:自體細胞療法(CAR-T,抽病人的免疫細胞出來培養之後打回去)。
規範醫療機構執行再生醫療技術(或)使用再生醫療製劑時,確保安全、品質及有效性,也限制臨床應用能執行再生醫療的範疇、再生醫療人體試驗及研究、組織細胞來源管理等等。
《再生醫療製劑管理條例》由衛福部食藥署(TFDA)主管,是管生技廠商和藥品的核准與否。
再生醫療雙法三讀版本的六大重點
重點一:限制異種細胞來源
恩慈療法排除異種細胞!
「鬼叔」:
恩慈療法可以用自體細胞療法(CAR-T, Autogenic)&異體細胞療法(抽「別人」的細胞來培養),如長聖的CAR001&UMSC01都是異體細胞療法(Allogenic),但是恩慈療法只能收成本費,對投資人不算利多!(異種細胞= 抽「其他動物」的細胞來培養,Xenogenic)
重點二:免人體試驗的規範和例外
除恩慈療法&原「特管法」核准的自體細胞療法(CAR-T)之外,必須完成人體試驗!

非恩慈療法之外的異體細胞療法必須完成人體試驗!要完成第幾期的人體試驗?哪些國家的人體試驗是台灣承認的?
需「於十大醫藥先進國家、地區已進行人體試驗」,確保一定安全下,才得例外免於國內進行或完成人體試驗。
此外,為滿足病人醫療迫切需求,《再生醫療製劑管理條例》也有規範,於完成第二期臨床試驗(Phase 2),並經審查風險效益,具安全性及初步療效者,可以核予業者有效期間不超過5年的有附款許可,應先經「再生醫療審議會」的審議通過。
審議會的職權範圍及成員組成,明確廣納相關專業領域人士,包括醫、藥、生技、倫理、法律與其他相關專業學者專家及病友團體,就再生醫療事項提供諮詢或審議。
「鬼叔」:
原「特管法」核准的自體細胞療法(CAR-T)= 包括癌症、膝關節軟骨缺損、難癒合的困難傷口等6項,只要衛福部醫事司審核通過,不須通過臨床試驗便可提供治療,其中以實體癌第四期(末期)的自體免疫細胞治療為最大宗。
十大醫藥先進國= 德國、美國、英國、法國、日本、瑞士、加拿大、澳洲、比利時、瑞典。這代表什麼?
如果有別家生技公司在以上這十個國家完成Phase 2的異體細胞療法,且安全有一定的療效,台灣的生技公司(如:長聖)就可以授權引進協助申請TFDA的accelerated approval,之後就可以開始用在病人身上!你不授權引進,人家也可以自己來申請喔,除了跟時間賽跑這還關乎到→得通路者得天下!
完成第二期臨床試驗= 美國FDA的accelerated approval,TFDA可以先給你5年的藥證,之後5年內要完成Phase 3就對啦!
至於應先經「再生醫療審議會」的審議通過才能核發藥證,已經完成Phase 2的clinical trial,不可能有違反倫理、法律的問題。所以,主要決定權還是在審議委員中的醫、藥、生技專家!就是說只要有初步療效,就會過關!
長聖的UMSC01治療急性心肌梗塞的異體細胞療法,Clinical trial上估2027年中完成Phase 2,41例隨機無盲,Phase 1時的8例沒有安全性上的問題!但是台灣的臨床試驗網站上是估2026/04/30完成!
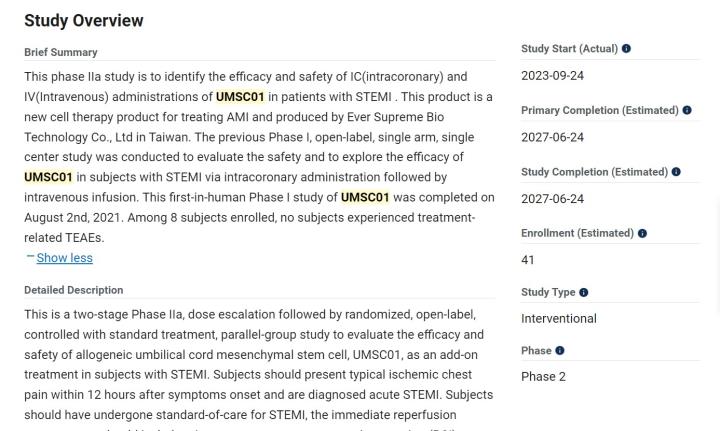

長聖的CAR001治療復發或難治型實體癌症的異體細胞療法(γδ T cells),2027年中完成Phase 2,非小細胞肺癌、三陰性乳癌、腦癌、大腸直腸癌共60例!(目前Clinical trial網站上尚未登錄已開始收案)
重點三:醫院不能成立再生醫療生技公司
「鬼叔」:
醫院不能成立,醫師可以成立呀!台灣人又不是傻子,長聖不就是這麼幹的嗎?
重點四:胎兒不得提供細胞及組織;無行為能力者的同意書應經公證始生效力!
「鬼叔」:像植物人的話,監護人的同意書要公證才生效,「公證」並不難呀!
重點五:胚胎幹細胞研究,不得製造雜交體、繁衍研究用的胚胎!
「鬼叔」:就是不能做複製人、狼人、美人魚、人面獅身…之類的!
重點六:每年要公開醫療機構的治療效果和統計醫療品質,如主管機關核准那幾家醫療機構執行、收案人數、不良事件、臨床療效(存活天數、傷口面積恢復多少…等)
「鬼叔」:老百姓最多只看的懂,那幾家醫院是合格被核准的、每年有多少人去該醫療機構治療、不良事件有幾件而已。真正關乎到療效的統計,是可以寫到你完全看不懂的!

「鬼叔」:「在這世上喔,你的老婆/老公會離開你,你的小孩也會離開你,只有統計不會離開你!」
同學:「為什麼?」
「鬼叔」:「因為統計,不會就是不會!」
橫批:一起致富
上聯:一個人走容易走歪
下聯:一群人走慢就是快
致富大道= 長期跟著成功者學習做人,緊緊追隨成效者經營人生,始終選擇與成果者合作方案!
季方案&年方案:https://www.cmoney.tw/app/ItemContent.aspx?id=5115
【免責聲明】
《鬼道》致富APP訂閱者必須完全瞭解,您所支付的訂閱費用是軟體APP的更新維護費用,與社團成員們在同學會和社團內的發文、互相分享、討論沒有任何對價關係。《鬼道》致富APP只是一款模擬台股的資料分析軟體,其中的選股策略及市場分析,僅是彙整部份投資相關書籍邏輯的研究心得。APP提供者並沒有對任何人,做任何真實股市中的買進(或)賣出建議。所有分析資料僅供參考,畢竟模擬與真實之間,必定存在極大的差異性!再者,相同的個股標的、相同的時間點、不同的人因為不同的心理抗壓素質,投資結果會完全不一樣。如果訂閱者自行套用在真實股市中,則必須清楚投資一定有風險,懇請審慎評估自身經濟條件及心理素質,並請自負盈虧,對自己的投資決策行為承擔所有責任!對訂閱者套用在真實股市中的投資決策行為,所導致之直接或間接損失,或因此產生之一切責任,《鬼道》致富APP提供者均不負任何損害賠償及其他法律上的責任。

 發表
發表


 我的網誌
我的網誌



