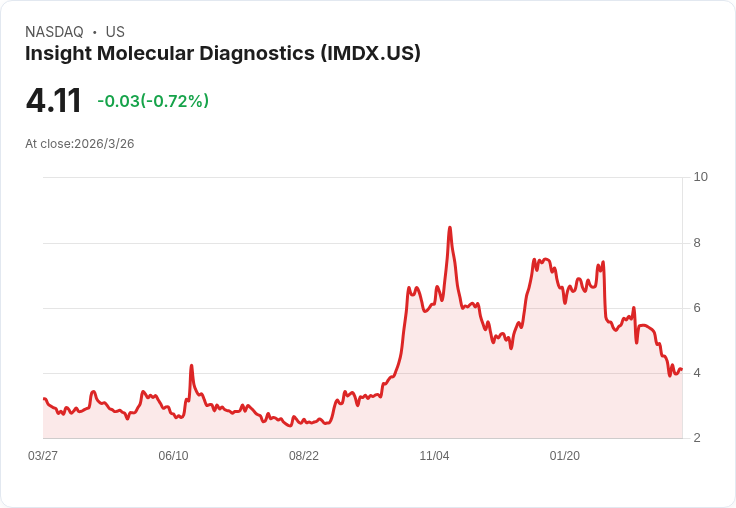
Insight Molecular Diagnostics 宣佈提交 GraftAssureDx 至 FDA,並計劃加速商業化程序,目標達成 20 億美元的市場潛力。
在最新的財報電話會議中,Insight Molecular Diagnostics Inc. (IMDX) 的首席執行官 Joshua Riggs 宣佈,公司已向美國食品藥品監督管理局(FDA)提交了 GraftAssureDx 的申請,這是第一款 dd-cfDNA 檢測工具。Riggs 強調,隨著授權後的推廣計畫,他們正迅速轉變為產品上市和商業化階段。自從去年秋天啟動註冊計畫以來,已有 28 家移植中心開始參與試驗,接近他們 50 家的目標。
公司計劃在未來一年內專注於擴大市場准入,包括推出僅供研究使用的 GraftAssure 和核心版本,並增加田納西州實驗室的樣本量。此外,GraftAssure 將被提交至英國及歐盟進行批准,並將研發重心轉向心臟移植檢測。CFO Andrea James 表示,公司估算總可用市場達到 20 億美元,而 Medicare 對 GraftAssure 的更新報銷金額為每次 $27.53。
展望未來,Insight Molecular Diagnostics 預計 2026 年的收入將相對低迷,但隨著實驗室服務的增長和商業化策略的落地,未來有望獲得穩健的收益。儘管面臨醫生採用新技術的挑戰,管理層仍然保持信心,認為 GraftAssureDx 有潛力成為市場上的標準檢測工具。在經過一系列的資本募集和數據驗證後,該公司正在全力以赴迎接即將到來的商業化浪潮。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37
 免責宣言
免責宣言
本網站所提供資訊僅供參考,並無任何推介買賣之意,投資人應自行承擔交易風險。

 發表
發表


 我的網誌
我的網誌